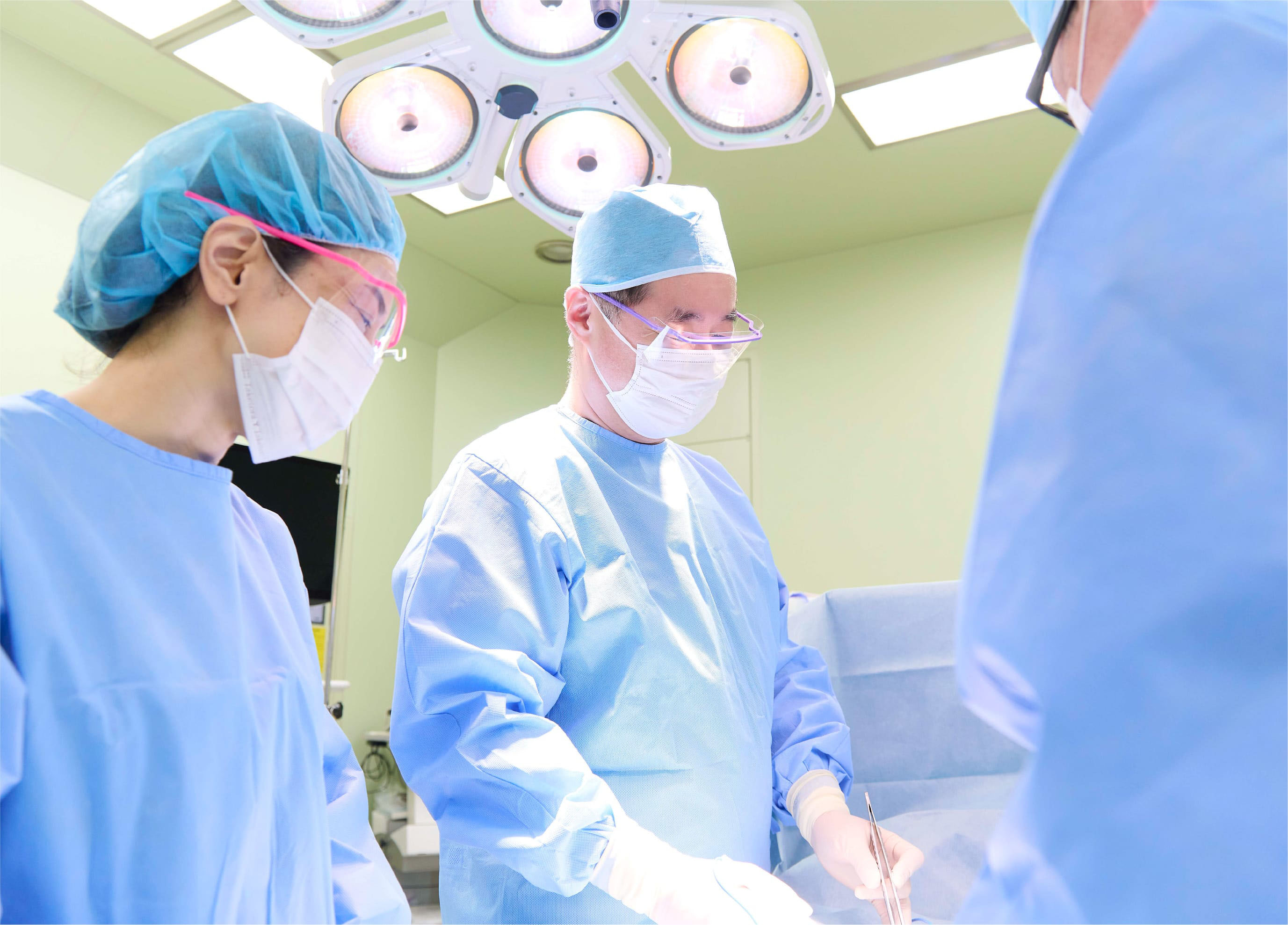
地域からのニーズに応え
スタンダードな医療を提供する
当院は開院当初から、医療を通じての地域への貢献を目指しております。医療体制が充実することで、この地域で救える命が増えました。また、治療できる医療機関がないため、一刻を争う状態の患者様の命を、ドクターヘリの利用や当院のドクターカーの出動等で、さらに広域から受け入れ、救うことが可能になりました。
これまでは柏・流山・松戸・野田・我孫子といった東葛北部医療圏5市の患者様を診療してきましたが、疾患によっては、 埼玉・茨城といった近隣県からも治療要請を受けています。

当院のご案内
診療のご案内
-
外来診療時間
午前8:30~11:50(診療開始9:00~)
午後13:00~16:50(診療開始14:00~)
※診療科により異なる場合があります -
面会時間
現在面会は予約制ととなっております
詳しくこちらはをご覧ください
-
休診日
土曜日(午後)・日曜日・祝日
年末年始(12月30日午後~1月3日)
コース紹介
人間ドック
- 人間ドック(3 大疾病コース・基本コース)
- 脳ドック(基本コース・簡易コース)
健康診断
- 各種健診 (特定健診・法定健診・雇用時健診 他)
- 柏市健診 (柏市特定健診・胃がん検診【内視鏡・バリウム】・乳がん検診・大腸がん検診)
(骨粗しょう症検査・肝炎ウィルス検査) - 特定保健指導
〒277-0863 千葉県柏市豊四季113
当院からのお知らせ

Access
交通アクセスについて